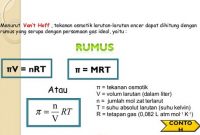
Rumusrumus.com kali ini akan membahas tentang rumus kimia asam klorida, beserta sifat kimia dan sifat fisika asam klorida serta fungsi dan kegunaannya.
Pengertian Asam Klorida
Asam klorida ialah larutan akuatik dari gas hidrogen klorida (HCl). asam klorida juga termasuk asam kuat, dan merupakan komponen utama di dalam asam lambung. Senyawa ini juga di pakai secara luas dalam industri. Asam klorida harus ditangani dengan memperhatikan keselamatan yang tepat dikarenakan merupakan cairan yang begitu sangat korosif.
Asam klorida juga pernah menjadi zat yang sangat begitu penting dan sering di pakai dalam awal sejarahnya. asam klorida ditemukan oleh alkimiawan Persia Abu Musa Jabir bin Hayyan pada sekitar tahun 800.
Senyawa ini digunakan sepanjang abad pertengahan oleh alkimiawan didalam pencariannya mencari batu filsuf, lalu digunakan juga pada ilmuwan Eropa termasuk Glauber, Priestley, dan Davy dalam rangka membangun pengetahuan kimia yang modern.
Rumus Kimia Asam Klorida
HCI dalam air H2O
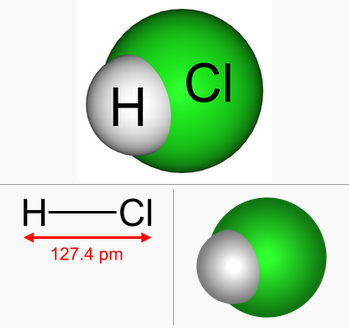
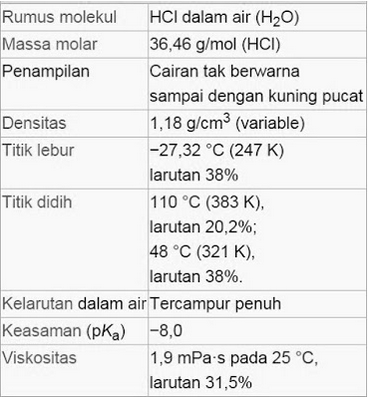
Sifat kimia asam klorida
Hidrogen klorida (HCl) ialah asam monoprotik, yang artinya bahwa ia dapat berdisosiasi melepaskan satu H+ sekali. Dalam larutan asam klorida, H+ ini bergabung dengan molekul air dan membentuk ion hidronium, H3O+:
HCl + H2O → H3O+ + Cl-
Ion lain yang terbentuk ialah ion klorida, Cl-. Asam klorida oleh karenanya bisa digunakan untuk membuat garam klorida, seperti misalnya natrium klorida. Asam klorida ialah asam kuat karena asam klorida berdisosiasi penuh dalam air.
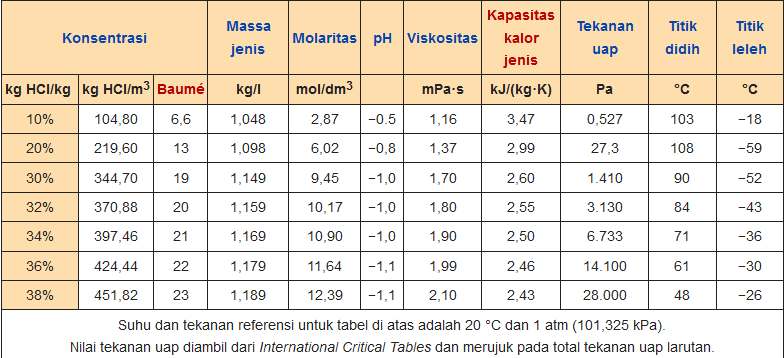
Sifat-Sifat fisika Asam Klorida
Sifat fisika asam klorida, seperti hal nya titik didih dan leleh, rapat jenis, dan pH, itu tergantung pada konsentrasi ataun molaritas HCI dalam larutan akuatik. berkisar dari konsentrasi yang begitu rendah mendekati 0% HCl sampai angka untuk asam klorida pekat berasap yakni lebih dari 40% HCl
Aplikasi
Asam klorida ialah asam anorganik kuat yang sering digunakan dalam berbagai macam proses industri , misalnya pengolahan logam. Aplikasi ini sering menentukan kualitas produk yang diperlukan
- Pengawetan baja
Salah satu aplikasi yang penting dari asam klorida ialah dalam pengawetan baja, untuk menghilangkan karat ataupun kerak oksida dari besi atau baja sebelum pengolahan selanjutnya, seperti rolling, ekstrusi, galvanisasi, dan teknik lainnya. HCl berderajat kemurnian teknis dengan konsentrasi 18% ialah yang paling umum dipakai sebagai pengawet untuk pengawetan baja karbon.
Fe2O3 + Fe + 6HCl → 3FeCl2 + 3H2O
Asam buangannya sudah sejak lama digunakan kembali sebagai larutan besi klorida (yang juga dikenal sebagai fero klorida),akan tetapi tingkat logam berat yang tinggi dalam cairan pengawet sudah menurun praktik ini.
Industri pengawetan baja sudah mengembangkan proses regenerasi asam klorida, seperti roaster semprot ataupun proses regenerasi HCl fluida, yang memungkinkan pemulihan HCI dari limbah bekas pengawetannya. Proses regenerasi yang paling biasa dipakai ialah proses pirohidrolisis, sesuai persamaan berikut:
4FeCl2 + 4H2O + O2 → 8HCl + 2Fe2O3
Dengan pemulihan asam bekas pengawetan, ditetapkan siklus asam tertutup. Besi oksida merupakan produk samping dari proses regenerasi yang berharga, yang dapat dipakai kedalam berbagai macam industri sekunder.
- Produksi senyawa organik
Penggunaan utama lainya pada asam klorida ialah dalam produksi senyawa organik, seperti dikloroetana dan vinil klorida untuk PVC. Ini ialah penggunaan yang pasti tetapi terbatas, mengkonsumsi secara lokal produk asam klorida yang tak pernah sampai ke pasar terbuka.
Senyawa organik lainnya yang di produksi dengan asam klorida ialah termasuk bisphenol A untuk polikarbonat, karbon aktif, dan asam askorbat, serta berbagai produk farmasi.
2CH2 = CH2 + 4HCl + O2 → 2ClCH2CH2Cl + H2O ( dikloroetana melalui oksiklorinasi )
kayu + HCl + panas → karbon aktif
Itulah pembahasan lengkap tentang ilmu kimia dari asam klorida semoga bermanfaat…
Artikel Lainnya :