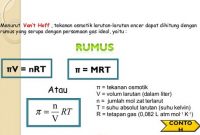
RumusRumus.com – kali ini akan membahas tentan rumus kimia nitrogen, pengertian nitrogen, isotop, serta kimia dan senyawa dan juga sejarah nitrogen.
Pengertian Nitrogen
Nitrogen ialah suatu unsur kimia di dalam tabel periodik yang mempunyai lambang N dan nomor atom 7.ditemukan sebagai gas yang tak ber warna, tak ber bau, tak ber rasa, dan merupakan gas diatomik non logam yang stabil, sangat sulit bereaksi dengan unsur atau senyawa lainnya. Diberi nama zat lemas karena zat ini bersifat malas, tak aktif bereaksi dengan unsur lainnya.
Rumus Nitrogen
Rumus kimia nitrogen ialah N dengan nomor atom 7
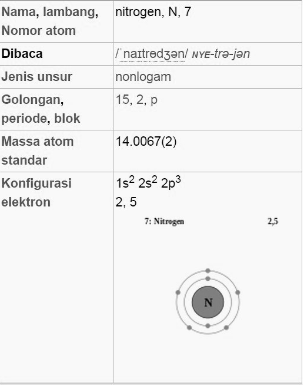
Isotop
Nitrogen mempunyai dua isotop yang stabi lyaitu 14N dan 15N. Isotop pertama lebih umum, menyusun 99,634% nitrogen alami, namun yang kedua (yang sedikit lebih berat) hanya sisanya 0,366%. Hal ini menyebabkan berat atomnya menjadi 14,007 u.
Kedua isotop stabil ini diproduksi melalui siklus CNO didalam bintang, akan tetapi 14N lebih umum terjadi karena tangkapan neutronnya ialah langkah pembatas laju. 14N ialah salah satu dari 5 nuklida ganjil–ganjil yang stabil (suatu nuklida yang mempunyai jumlah proton dan neutron ganjil) empat lainnya ialah 10B, 2H, 6Li, dan 180mTa.
Kelimpahan relatif 14N dan 15N nyaris konstan di atmosfer, akan tetapi bisa bervariasi di tempat lain, dikarenakan fraksinasi isotop alami dari reaksi redoks biologis dan penguapan amonia ataupun asam nitrat alami.
Reaksi yang dimediasi akan secara biologis (contohnya asimilasi, nitrifikasi, maupun denitrifikasi) sangat mengendalikan dinamika nitrogen dalam tanah. Reaksi ini biasanya menghasilkan pengayaan 15N dari substrat dan penipisan produk

Kimia dan Senyawa
Nitrogen atom, yang juga dikenal sebagai nitrogen aktif, sangat reaktif, berbentuk triradikal dan dengan tiga elektron yang tak berpasangan. Atom nitrogen bebas sangat mudah bereaksi dengan sebagian besar unsur untuk membentuk nitrida, dan bahkan ketika dua atom nitrogen – bebas bertumbukan untuk menghasilkan molekul molekul N2 yang tereksitasi, mereka dapat melepaskan banyak energi pada tumbukan dengan molekul stabil semacam karbondioksida dan air yang menyebabkan fisi homolitik yang menghasilkan radikal seperti CO dan O ataupun OH dan H.
Nitrogen atomik disiapkan dengan melewatkan aliran listrik melalui gas nitrogen pada 0,1–2 mmHg, yang menghasilkan nitrogen atom bersamaan dengan emisi kuning peach dan memudar perlahan sebagai pendaran beberapa menit bahkan setelah aliranlistrik
Hidrida utama nitrogen yaitu amonia (NH3) meskipun hidrazina (N2H4) juga banyak ditemukan. Amonia memiliki sifat basa dan terlarut sebagian dalam air membentuk ion ammonium (NH4+). Amonia cair sebenarnya sedikit amfiprotik lalu membentuk ion ammonium, dan amida (NH2-) dikenal juga sebagai garam amida, dan nitrida (N3-), tetapi terurai dalam air.
Gugus bebas amonia dengan atom hidrogen tunggal ataupun ganda diberi nama amina. Rantai, cincin atau struktur hidrida nitrogen yang lebih besar diketahui tetapi tak stabil
Sejarah Nitrogen
Unsur nitrogen ini pertama kali ditemukan dan diisolasi oleh dokter yang berkebangsaan Skotlandia yaitu Daniel Rutherford pada tahun 1772. walaupun Carl Wilhelm Scheele dan Henry Cavendish secara terpisah sudah melakukan hal yang sama di kisaran waktu yang sama juga, Rutherford secara umum sesuai untuk menerima penghargaan tersebut dikarenakan karyanya yang dipublikasikan pertama kali.
Nama nitrogen diusulkan oleh Jean-Antoine-Claude Chaptal pada tahun 1790, saat ia menemukan bahwasanya nitrogen hadir dalam asam nitrat dan nitrat . Antoine Lavoisier justru mengusulkan nama azote, dari bahasa Yunani άζωτικός y ang artinhyatak hidup, karena unsur itu termasuk gas asfiksia; nama usulan Lavoisier justru digunakan di banyak bahasa, seperti Perancis, Rusia, mauupun Turki, dan muncul dalam dua nama bahasa Inggris untuk beberapa senyawa nitrogen seperti hidrazin, azo maupun azida.
Artikel Terkait :